Granulocyte受体
粒细胞是由造血干细胞的粒细胞系发育而来,胞质内含有许多颗粒,是最常见的白细胞类型。粒细胞在骨髓内成熟后即移入血循环,并可逸出血管壁进入组织内或炎症部位、渗出液及体液中。但离开血液的粒细胞不能再重新返血循环。粒细胞可通过瑞氏染料染色分为:中性粒细胞、嗜酸性粒细胞和嗜碱性粒细胞三种细胞类型。不同类型粒细胞表面的膜蛋白分子不尽相同,即为粒细胞受体。
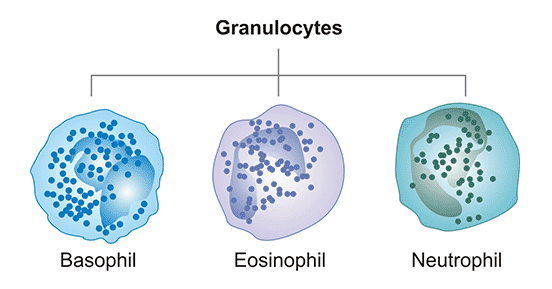
图1. 三种粒细胞示意图
1、中性粒细胞受体
中性粒细胞(Neutrophils)受体指的是在中性粒细胞表面表达的一系列膜蛋白,包括FcγR、多种趋化因子受体(IL-8R等)和补体受体(C5aR/C3bR/C4bR等),赋予了中性粒细胞很强的趋化和吞噬能力。通过吞噬病原体,以胞内颗粒(髓过氧化物酶、酸性磷酸酶、溶菌酶、碱性溶菌酶和防御素等)和形成细胞外陷阱等多种方式杀灭人侵微生物。同时,还可释放白三烯啸酸性粒细胞趋化因子,激肽酶原等多种炎症介质而引起炎症反应[1]。
在瑞氏染色血涂片中,中性粒细胞(Neutrophils)胞质呈无色或极浅的淡红色,有许多弥散分布的细小浅红或浅紫色的特有颗粒。据估计,人类和小鼠每天分别产生1011和107个中性粒细胞,从最后一次骨髓细胞分裂到释放入循环中的时间分别是6~7d和3d。中性粒细胞从循环系统进入组织,在宿主防御中起重要作用,具有保护人体先天和适应性免疫的效应功能,是炎症和感染的第一反应者[2] [3]。
2、嗜酸性粒细胞受体
嗜酸性粒细胞(Eosinophils)受体指的是在嗜酸性粒细胞表面表达的一系列膜蛋白,比如免疫球蛋白Fc片断和补体C3的受体。这类受体可在已经对某种蠕虫具有免疫性的动物体内,产生了特异性的免疫球蛋白IgE。蠕虫经过特异性IgE和C3的调理作用后,嗜酸性粒细胞可借助于细胞表现的Fc受体和C3受体粘着于蠕虫上,并且利用细胞溶酶体内所含的过多氧化物酶等酶类损伤蠕虫体。此外,嗜酸性粒细胞的颗粒中包含了特殊的毒性蛋白以及组织蛋白酶,在杀灭如寄生性线虫等寄生虫的过程中扮演了重要的角色。
3、嗜碱性粒细胞受体
嗜碱性粒细胞(Basophils)受体指的是在嗜碱性粒细胞表面表达的一系列膜蛋白,比如IgE受体FcεRI、CD49b、c-kit和与固有免疫相关的免疫分子等。嗜碱性粒细胞表面与固有免疫相关的免疫分子包括模式识别受体如Toll样受体、补体受体以及蛋白酶激活受体等。这些受体与相应配体结合,并随之释放IL-4、IL-13等Th2类细胞因子、趋化因子等,启动变应原特异性Th2免疫应答,参与免疫调节。IL-4与IL-13参与过敏性疾病及炎症反应过程,且在固有免疫及适应性免疫发挥重要防御作用。故嗜碱性粒细胞除了参与急性及慢性炎症反应、抗寄生虫免疫,而且参与调节固有免疫及获得性免疫。
4、热门粒细胞受体相关靶点
j9九游会登录入口首页生物罗列了部分热门粒细胞受体相关靶点,点击对应靶点可查看该靶点相关的所有试剂。
- C3AR1
- C5AR1
- CCR1
- CCR2
- CCR3
- CCR4
- CCR6
- CCR8
- CSF2RA
- CSF2RB
- CSF3R
- CXCR1
- CXCR2
- CXCR3
- CXCR4
- CXCR5
- FCER1A
- FCGR2A
- FCGR2B
- FCRL5
- FLT3
- IFNAR1
- IFNAR2
- IFNGR1
- IFNGR2
- IL10RA
- IL10RB
- IL13RA1
- IL13RA2
- IL15RA
- IL17RA
- IL18R1
- IL1R1
- IL1R2
- IL3RA
- IL4R
- IL5RA
- IL6R
- IL6ST
- IL7R
- IL9R
- PTGDR2
- PTPRC
- TLR1
- TLR2
- TLR4
- TLR5
- TLR6
- TLR8
- TLR9
- TNFRSF13C
- TNFRSF14
- TNFRSF1A
- TNFRSF1B
参考文献:
[1] Coffelt SB, Wellenstein MD, de Visser KE. Neutrophils in cancer: neutral no more [J]. Nat Rev Cancer. 2016, 16(7): 431-446.
[2] Mao FY, Zhao VL, Lv YP, et al. myeloid-derived suppressor cells suppress CD8+ T cell activity via the IL-6/TL-8-arginase I axis in human gastric cancer [J]. Cell Death Dis. 2018, 9(7): 763.
[3] Brinkmann V, Reichard U, Goosmann C, et al. Neutrophil extracellular traps kill bacteria [J]. Science. 2004, 303 (5663): 1532-1535.






