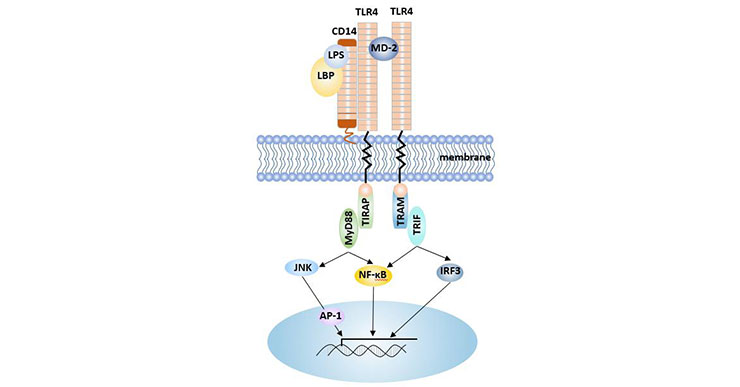
CD14—细菌脂多糖的膜受体
日期:2019-08-29 11:44:35
CD14(cluster of differentiation 14)原称MY23抗原,是一种表面抗原,属细胞表面糖蛋白家族成员之一。CD14基因编码的蛋白,优先表达于单核/巨噬细胞。CD14是革兰阴性菌内毒素脂多糖LPS和LPS结合蛋白(LBP)复合物的高亲和力受体。CD14识别并结合LPS,引起细胞酪氨酸磷酸化、核因子NF-κB转位、触发细胞因子释放和氧自由基产生,在机体免疫、防御系统引起的一系列反应中发挥重要作用。
1. CD14的发现
1981年,Todd首次从人单核细胞表面发现了CD14。1985年,Maliszewski从人血清中发现了可溶性CD14[1],它与之前发现的单核细胞表面的CD14结构相似[2]。1990年,CD14被发现可作为LPS/LPS结合蛋白复合物的受体,介导LPS性细胞反应[3]。
2. CD14的分类
CD14以两种形式存在,一种是细胞膜CD14,通过糖基磷脂酰肌醇尾部(mCD14)固定在膜上,另一种是可溶性形式(sCD14)。
mCD14是一种55 kDa的糖蛋白,不含跨膜区。
sCD14相比mCD14而言,其分子量较小,因为其缺少PI结构[4]。可溶性CD14分为两种:sCD14α和sCD14β,它们的分子量分别为49 kDa和55 kDa[5]。
单核细胞产生sCD14的方式可能有两种:
由mCD14在蛋白酶或磷脂酶催化分解作用下(脱去PI成分)脱落而成。
由CD14基因转录、合成的CD14蛋白,不进行PI化或逃脱PI化,最后经由细胞内囊泡分泌。
3. CD14的结构特点
CD14基因位于人类5号染色体长臂5q23-31区,约3900 bp。
人CD14的前体蛋白多肽链由375个氨基酸组成,通过将前体多肽的前19位信号肽去除而形成成熟的由356个氨基酸组成膜型CD14,其分子量为55 kD。
N-末端的第39-44位残基是人类CD14与LPS结合位点的最基本部分,第86-329位残基间包含10个富含亮氨酸的重复特征性序列[6],可与脂类作用形成亲水的β折叠,可能在蛋白质与蛋白质的识别中起重要作用。CD14氨基酸序列羧基末端含有17个疏水性中性氨基酸,并有5个N-糖基结合位点。
人和鼠CD14成熟蛋白质共有的特征为:
含有大量的亮氨酸;
有多个N-糖苷键;
有数个半胱氨酸残基;
分子中央部分有以亮氨酸为主的重复序列。
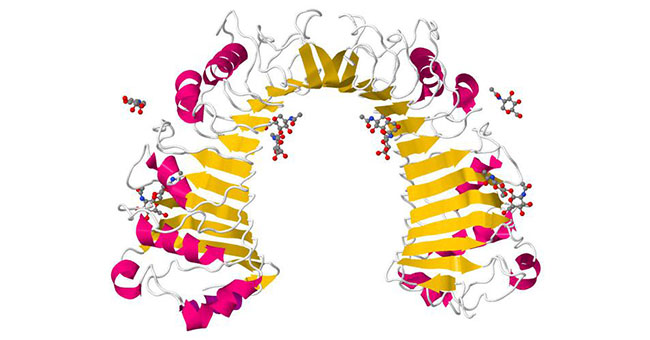
图1 CD14的结构
该图片来自维基百科
4. 组织分布
CD14在人和鼠体内表达具有组织特异性和细胞特异性。
mCD14主要分布在单核细胞,巨噬细胞和树突细胞的细胞表面,因此CD14(mCD14)可作为辨别单核细胞或巨噬细胞的一个有用标志。此外,mCD14还存在于中性粒细胞胞浆内膜性分泌小体和嗜苯胺兰颗粒中[7],而内皮细胞、上皮细胞等表面则未发现mCD14的存在。
sCD14则存在于正常人和动物的血浆(清)中,人血清中sCD14的正常浓度为2~5 mg/ mL,占血中全部CD14含量的99%。sCD14还微量存在于尿液。
5. 配体
mCD14位于免疫效应细胞表面,其配体包括脂多糖(LPS)、肽多糖、磷壁酸、脂肽和多种其他微生物信号。此外,mCD14也能识别热休克蛋白60、神经酰胺、磷脂类、脂蛋白等内源性配体。CD14也是革兰氏阳性菌细胞壁成分肽聚糖(peptidoglycan, PGN)、分枝杆菌上的脂阿拉伯甘露糖(lipoarabinomannan)及多种病原体的受体[8]。
6. CD14的功能
CD14是一种锚定蛋白,是一种普遍存在的模式识别受体。CD14作为细菌脂多糖LPS的细胞膜受体,它与其他蛋白质协同作用,在机体免疫、防御系统引起的一系列病理反应中起关键作用。
mCD14:在单核细胞、巨噬细胞和中性粒细胞等具有mCD14的细胞中,mCD14在受到其配体LPS/LBP的作用后,可使靶细胞产生细胞因子,从而诱发机体产生免疫应答和病理性损伤。mCD14刺激单核细胞等分泌TNF、IL-1等细胞因子。
mCD14刺激巨噬细胞产生FGF、转化生长因子-β (TGF-β)、PDGF,它们均可诱发细胞的生长。
CD14除作为LPS受体参与细胞活化之外,还有其它功能。CD14是巨噬细胞上识别和吞噬凋亡细胞的受体之一。研究认为,CD14可能作为一个信号识别分子,和其他受体CR3(CD11b/CD18),CR4(CD11c/CD18)联合激活信号,介导凋亡。
CD14在巨噬细胞识别、吞噬凋亡细胞中的作用依赖于CD14的一个区域,这个区域与LPS的结合区域紧密相关。
sCD14:可溶性CD14(sCD14)与细胞膜CD14竞争结合LPS,并介导不表达CD14的内皮细胞和平滑肌细胞对LPS的应答。可溶性CD14与LPS结合在不同的浓度条件下发挥不同的生理功能。在生理浓度下,sCD14作为LPS激动剂发挥作用,在较高浓度下,sCD14则发挥LPS拮抗作用。比如,血中sCD14浓度增高可减少LPS/LBP复合物与单核细胞结合,进一步减少炎症因子的生成,从而对炎症反应进行调控[9]。
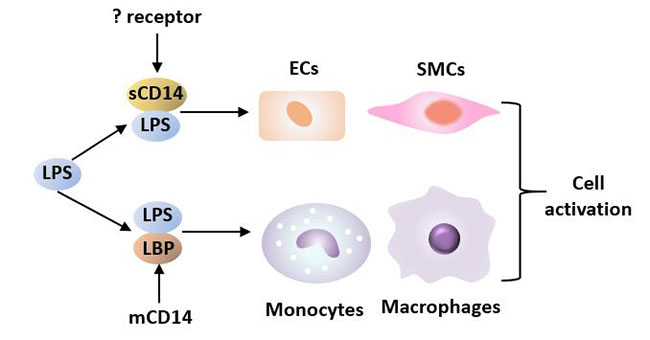
图2 LPS与LBP、CD14相互作用诱导细胞活化
7. CD14介导的信号通路
CD14与LPS信号转导主要包括跨膜信号转导和细胞内信号转导。
7.1 CD14跨膜传导途径
CD14跨膜传导途径有3种模式[10]:
模式I为单构件受体信号受体模式:即LPS(LPS/LBP)与mCD14连接后开始传导信号,信号传递到细胞时,由跨膜蛋白识别;另外两种模式则认为LPS受体是多构件受体,包含配体结合亚单位mCD14和跨膜蛋白传递信号,这些模式认为CD14在细胞与LPS结合上起重要作用,但在跨膜信号传导中需要有附加蛋白参与。
LPS多以多聚体的形式存在于水溶液中,并且以低速解聚成单体。LBP可以识别LPS,加快LPS多聚体的解聚。LBP可以与LPS单体结合并将LPS运送至髓源性细胞表面,与髓源性细胞表面的mCD14结合,形成LPS-LBP-CD14三联复合体。该三联复合体被转运至TLR4-MD2蛋白复合体处,在MD-2的帮助下与TLR4结合,激活TLR4,使之二聚化。TLR4可以介导与下游蛋白激酶的相互作用[11]。
TLR4-MD2也是toll样信号通路的重要组成部分,说明CD14与toll样信号通路具有很强的相关性。
7.2 细胞内信号传递
信号传至胞内后,通过酪氨酸蛋白激酶激活胞内髓样分化因子(myeloid differentiation factor 88,MyD88),随后通过磷酸化IRAK-1将信号传给肿瘤坏死因子受体相关因子6(TRAF6),使之活化。活化的TRAF6通过激活核因子κB诱导激酶(NIK)和转化生长因子β活化的激酶(TAK1),从而激活相应的NF-κB和丝裂原活化蛋白激酶(MAPK)两条通路。
8. 疾病
CD14与多种疾病相关,在宿主抗感染中发挥双重作用,这取决于其微生物类型及其表达的病原体相关的分子模式(PAMPs)。CD14扩增反应可以通过诱导足够的炎症和免疫反应来消灭入侵的微生物,从而对宿主有益。它也可因过度炎症和/或病原体的传播,从而能对宿主造成不利的影响。
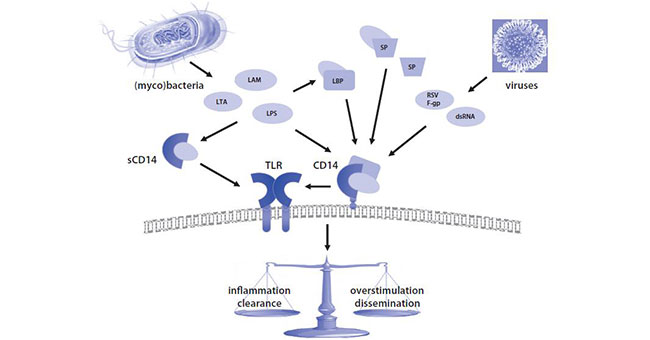
图4 CD14在病原体和病原体相关分子模式(PAMP)诱导的肺部反应中的作[13]
8.1 脓毒症
脓毒症(sepsis)是指由感染引起的全身炎症反应综合征,是创伤、烧伤、休克、感染等临床急危重患者的严重并发症之一,也是诱发脓毒性休克、多器官功能障碍综合征的重要原因。脓毒症主要是由炎症反应的失衡造成的。LPS是全身炎症反应的重要触发剂,它与脓毒症、重症脓毒症以及脓毒性休克的炎症过程密切相关。
高浓度的sCD14与由革兰染色阴性菌引起的脓毒血症的死亡率增加有关[14]。研究表明,脓毒症患者血浆中sCD14水平明显升高,mCD14水平明显下降,且这种变化与疾病的严重程度及预后相关。血清sCD14是革兰氏阳性脓毒症的良好预后指标,其水平升高与高死亡率相关。研究显示[15],sCD14亚型Presepsin作为一种新型脓毒症生物标记物,在感染患者中,其血浆浓度明显高于非感染患者,且Presepsin在脓毒症的早期诊断、严重性评估和预后方面均优于PCT、CRP、IL-6传统标志物,具有较高的敏感性,有望成为理想的脓毒症生物标记物。但其缺点是特异性不足[16]。
8.2 免疫系统疾病
自身免疫性疾病的患者,外周血中sCD14明显升高,细胞mCD14表达增加。当患者接受激素类药物治疗时,外周血中sCD14水平及单核细胞mCD14的表达均受抑制。
8.3 心血管系统疾病
sCD14促使内皮细胞活化,可加速动脉粥样硬化斑块的形成。单核细胞表面的CD14与LPS结合可引起单核细胞的活化,同样可加速或促进动脉粥样硬化的形成[17]。CD14是一种很重要的风险因素,它在引起动脉粥样硬化的过程中起着重要作用[18]。sCD14水平升高与主动脉硬化、颈动脉斑块形成、不稳定型心绞痛密切相关[19]。
此外CD14在调节树突细胞凋亡、预测心血管事件及评估慢性肾脏疾病预后中起着重要作用。高浓度的sCD14与艾滋病患者逐渐增加的死亡率有关;
CD14 mRNA和TLR4 mRNA表达与PD患者疾病严重程度有一定关系,提示机体固有免疫可能参与了PD的发生发展。
CD14是RA发生及发展的相关基因[20]。单核细胞表面受体CD14与慢性炎症的发生和维持有关。
CD14与慢性肾病(CKD)有密切关系。
最新研究进展
Chakraborty[21]等人于2018年发表在杂志EBioMedicine上的文章表明CD14在恶性疟原虫疟疾中起主导作用。它通过证明该启动子多态性的顺式调节作用,为rs5744454与恶性疟原虫严重疟疾的遗传关联建立了功能基础。此外,该研究还为基于青蒿素的抗疟疾治疗指明了一个新的方向。
Bedell等人[22]于2018年发表在杂志Biomaterials上的文章表明在血液来源的细胞中靶向CD14可改善皮质内微电极性能,而提高皮质内微电极性能,则可能克服跨越血脑屏障进行治疗这一难关。
Reference:
[1] Todd R F, Nadler L M, Schlossman S F. Antigens on human monocytes identified by monoclonal antibodies [J]. Journal of Immunology, 1981, 126(4): 1435-1442.
[2] Maliszewski C R, Currier J, Fisher J, et al. Monoclonal antibodies that bind to the My23 human myeloid cell surface molecule: Epitope analysis and antigen modulation studies [J]. Molecular Immunology, 1987, 24(1): 17-25.
[3] Wright S, Ramos R, Tobias P, et al. CD14, a receptor for complexes of lipopolysaccharide (LPS) and LPS binding protein [J]. Science, 1990, 249(4975): 1431-1433.
[4] Frey E A, Miller D S, Jahr T G, et al. Soluble CD14 participates in the response of cells to lipopolysaccharide [J]. Journal of Experimental Medicine, 1993, 176(6): 1665-1671.
[5] Landmann R, Zimmerli W, Sansano S, et al. Increased Circulating Soluble Cd14 Is Associated With High Mortality In Gram-Negative Septic Shock [J]. Journal of Infectious Diseases, 1995, 171(3): 639-644.
[6] Viriyakosol S, Kirkland T N. The N-terminal half of membrane CD14 is a functional cellular lipopolysaccharide receptor [J]. Infection & Immunity, 1996, 64(2): 653-6.
[7] Fearns C, Ulevitch R J. EFFECT OF RECOMBINANT INTERLEUKIN-1β ON MURINE CD14 GENE EXPRESSION IN VIVO [J]. Shock, 1998, 9(3): 157-163.
[8] Tobias P S, Gegner J, Tapping R, et al. Lipopolysaccharide dependent cellular activation [J]. Journal of Periodontal Research, 1997, 32(1): 99-103.
[9] Bazil V, Strominger J L. Shedding as a mechanism of down-modulation of CD14 on stimulated human monocytes [J]. Journal of immunology, 1991, 147(5): 1567-1574.
[10] Ulevitch R J, Tobias P S. Receptor-Dependent Mechanisms of Cell Stimulation by Bacterial Endotoxin [J]. Annual Review of Immunology, 1995, 13(1): 437-457.
[11] Botos I, Segal D, Davies D. The Structural Biology of Toll-like Receptors [J]. Structure, 2011, 19(4): 447-459.
[12] Martel G, Rousseau S. TPL2 signalling: From Toll-like receptors-mediated ERK1/ERK2 activation to Cystic Fibrosis lung disease [J]. The International Journal of Biochemistry & Cell Biology, 2014, 52: 146-151.
[13] Anas A, Van d P T, de Vos A F. Role of CD14 in Lung Inflammation and Infection [M]. Intensive Care Medicine. Springer New York, 2010.
[14] Olad E, Sedighi I, Mehrvar A, et al. Presepsin (Scd14) as a Marker of Serious Bacterial Infections in Chemotherapy Induced Severe Neutropenia [J]. Iranian Journal of Pediatrics, 2014, 24(6): 715.
[15] Endo S, Suzuki Y, Takahashi G, et al. Usefulness of presepsin in the diagnosis of sepsis in a multicenter prospective study [J]. Journal of Infection and Chemotherapy, 2012, 18(6): 891-897.
[16] Liu B, Chen Y X, Yin Q, et al. Diagnostic value and prognostic evaluation of Presepsin for sepsis in an emergency department [J]. Critical Care, 2013, 17(5): R244
[17] Hubacek J A, Rothe G, Pitha J, et al. C(-260)-->T polymorphism in the promoter of the CD14 monocyte receptor gene as a risk factor for myocardial infarction [J]. Circulation, 1999, 99(25): 3218-3220.
[18] Kitchens R L, Thompson P A. Viriyakosol S, et al. Plasma CD14 decreases monocyte responses to LPS by transferring cell-bound LPS to plasma lipoproteins [J]. Journal of Clinical Investigation, 2001, 108(3): 485-493.
[19] Reiner A P, Lange E M, Jenny N S, et al. Soluble CD14: Genomewide Association Analysis and Relationship to Cardiovascular Risk and Mortality in Older Adults [J]. Arteriosclerosis, Thrombosis, and Vascular Biology, 2013, 33(1): 158-164.
[20] Fontaine L D L, Schwarz M J, Riedel M, et al. Investigating disease susceptibility and the negative correlation of schizophrenia and rheumatoid arthritis focusing on MIF and CD14 gene polymorphisms [J]. Psychiatry Research, 2006, 144(1): 0-47.
21] Chakraborty B, Mondal P, Gajendra P, et al. Deciphering genetic regulation of CD14 by SP1 through characterization of peripheral blood mononuclear transcriptome of P. faiciparum and P. vivax infected malaria patients [J]. EBioMedicine, 2018.
[22] Bedell H W, Hermann J K, Ravikumar M, et al. Targeting CD14 on blood derived cells improves intracortical microelectrode performance [J]. Biomaterials, 2018, 163: 163-173.
上一篇: 生长激素-不仅仅促进长高