CCR8:Tregs细胞的特异性靶点,催生下一代重磅肿瘤免疫药物!
日期:2021-11-10 10:18:50
继PD-(L)1大获成功之后,肿瘤免疫治疗取得了革命性的成功,但肿瘤组织中浸润了大量的免疫抑制性细胞,使得不同类型肿瘤患者对肿瘤免疫疗法的应答率较低。对于实体瘤治疗而言,为提高治疗效果,最重要的方面是解除肿瘤微环境(TME)对免疫效应细胞的抑制作用。因此,开发出特异性靶向和清除肿瘤组织中浸润的调节性T细胞(Tregs),是突破PD-1局限性的必然方向。
Tregs已被证明在肿瘤免疫中发挥重要作用,其主要功能是抑制自身反应性细胞介导的病理性免疫应答。随着肿瘤相关Tregs标记物CTLA4和CCR4药物的上市,CCR8的出现更是引起了广泛的重视,CCR8这个过去几乎无人问津的靶点走到了抗肿瘤新药研发的前沿,点燃了各大制药企业对它的研发热情。
CCR8靶点的发光之旅
2020年9月1日,吉利德Gilead宣布以8.05亿美元从Jounce Therapeutics获得CCR8靶向抗体JTX-1811的合作开发权。正因这场不菲协议的达成,Jounce估价飙升了70%。与此同时,CCR8正式步入人们视野。
2020年9月2日,上海和铂医药公司在第16届蛋白质工程峰会(PEGS)以口头汇报的形式,展示其针对CCR8靶点开发的单克隆抗体HBM1022,预期将于2022年提交HBM1022的临床试验申请(IND)申请;
2021年2月,Vaccinex宣布Surface Oncology获得CCR8抗体(SRF114)开发的权益,当月,Surface Oncology的股价大幅上涨。目前,Surface Oncology市值达33亿美元;
2021年2月,安进Amgen以19亿美元收购Five Prime,以扩大肿瘤产品管线,Five Prime的产品就包括CCR8单抗FPA157,预计将在2022年上半年提交IND;
2021年5月,Bristol-Myers Squibb(BMS),启动了一项CCR8靶向单克隆抗体BMS-986340的临床试验,以评估其与O类药物联合治疗多种实体肿瘤的疗效;
2021年8月,南京艾美斐医药宣布,自主研发的靶向CCR8小分子抑制剂(IPG7236)的IND获得FDA批准。今年9月,艾美斐医药完成1亿元A+轮融资,将用于IPG7236的I期临床试验的开展和商业化准备;
有理由相信,国内外生物制药公司对CCR8的关注将持续上升。
CCR8靶点简介
CCR8是趋化因子受体亚家族的成员之一,属于G蛋白偶联受体。人CCL1是CCR8的主要配体,其它配体有CCL8、CCL16和CCL18。CCR8在肿瘤浸润的调节性T细胞(Treg)上特异性表达,在Th2细胞和肿瘤细胞也均有表达;然而在外周血Treg或正常组织上基本不表达。CCR8的主要作用是参与Tregs和Th2细胞向炎症和肿瘤部位的募集。大量研究发现,高表达的CCR8与多种癌症相关,包括结直肠癌、乳腺癌、胃癌、转移性脑癌、转移性肝癌,尤其是在乳腺癌分离的Tregs细胞上,所以近几年研究人员的目光开始聚集在CCR8身上。
CCR8+Tregs在TME中的浸润机制
在解释该机制前,我们先了解一个概念,什么是调节性T细胞(Tregs)?Tregs是一种特殊的CD4阳性淋巴细胞亚群,具有免疫调节功能,能够抑制过度和不受控制的免疫反应。最重要的是,Tregs通过抑制攻击肿瘤的免疫细胞的免疫反应,在肿瘤免疫逃避中发挥关键作用。
具体看看CCR8+Tregs是如何在TME是发挥作用的,如图1,肿瘤干细胞CAF和TAM分泌CCL1到TME中,与多种细胞上的CCR8结合并激活CCR8。CCR8-CCL1轴的作用主要包括:1. CCL1结合肿瘤细胞上的CCR8,引起肿瘤细胞增殖,迁移和抗细胞凋亡;2. CCL1结合血管内皮细胞上的CCR8,促血管生成以及肿瘤生长;3. CCL1结合CD4+T细胞上的CCR8,导致CD4+T细胞转化为Tregs,再募集Tregs;4. CCL1结合Tregs上的CCR8,Tregs向炎症或肿瘤部位募集。
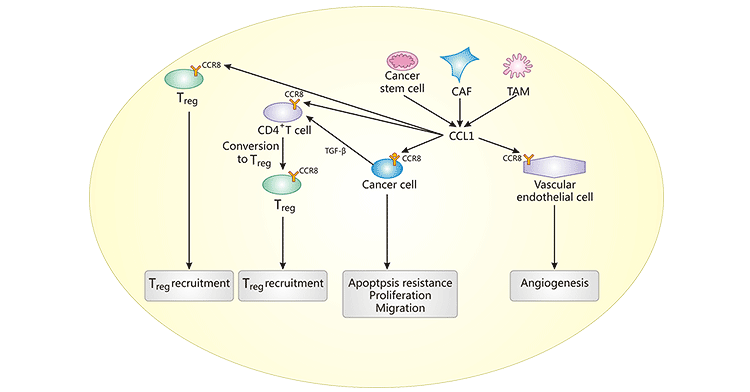
图1. CCR8-CCL1轴的作用
CCR8-CCL1轴不仅将CCR8+Tregs招募到TME中,如图2,CCR8-CCL1还可诱导对Tregs抑制至关重要的FOXP3和CD39,以及IL-10的上调,这将增强Treg的免疫抑制活性。研究发现,与正常组织中的Tregs相比,CCR8在人类乳腺癌的肿瘤浸润性Tregs中显著上调,表明CCR8是TME中Tregs上的一个有希望的治疗靶点,而不会引起系统性自身免疫。因此,以CCR8为靶点的抗体,清除肿瘤微环境中的Treg细胞,将改善TME的免疫功能。
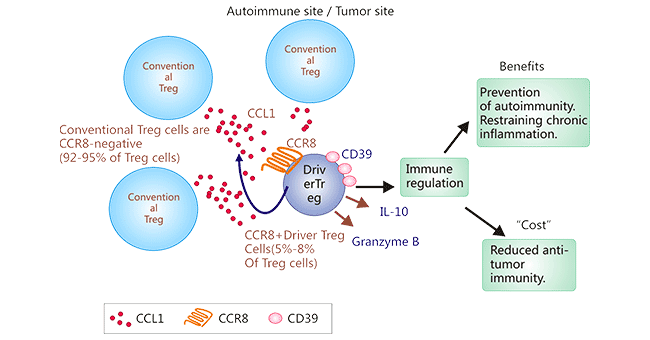
图2. CCR8+Tregs在TME中的浸润机制
CCR8靶点在研项目
截止目前,可查到信息的CCR8靶点在研项目有6个,这跟其研究尚在早期有关。国外药企有吉利德、BMS、Five Prime(已被安进Amgen收购);国内,和铂医药和艾美斐生物医药已开始布局。此外,通过专利检索得到,国内一家普米斯生物关于CCR8已申请CCR8单抗和CCR8xCTLA-4双抗2个专利。不难看出,CRR8将一个极具潜力的免疫治疗靶点,未来我们或将看到更多的CCR8单抗或双抗的药企玩家。
| 药物名称 | 研发状态 | 公司 | 治疗领域/适应症 | 最后更新日期 |
|---|---|---|---|---|
| JTX-1811 GS-1811 |
临床一期 | Gilead Sciences Inc | 实体瘤 | 2021-08-26 |
| IPG-7236 | 临床阶段不明 | 南京艾美斐生物医药科技有限公司 | 实体瘤 | 2021-08-20 |
| SRF-114 | 临床前 | Surface Oncology | 肿瘤 | 2021-08-24 |
| FPA-157 | 临床前 | Five Prime Therapeutics Amgen | 实体瘤 | 2021-08-24 |
| HBM-1022 | 临床前 | 和铂医药 | 肿瘤 | 2021-08-24 |
| BMS-986340 | 临床前 | Bristol-Myers Squibb Srl | 肿瘤 | 2021-08-24 |
数据来源药渡
为鼎力协助各药企在CCR8靶点上的研发,j9九游会登录入口首页科赛博推出CCR8活性蛋白产品,欢迎联系我们。
Recombinant Human CCR8-VLPs 活性蛋白实验验证数据
● 经WB验证蛋白特异性

CSB-MP004847HU is detected by Mouse anti-6*His monoclonal antibody.
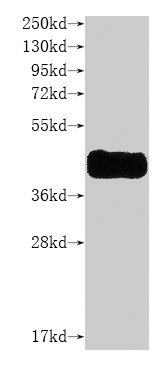
CSB-MP004847HU is detected by Anti-CCR8 recombinant Antibody
● 功能性ELISA验证高活性

Immobilized human CCR8 at 5 μg/ml can bind Anti-CCR8 recombinant Antibody. The EC50 is 11.13-17.29 ng/mL.
● 经TEM验证蛋白正确组装
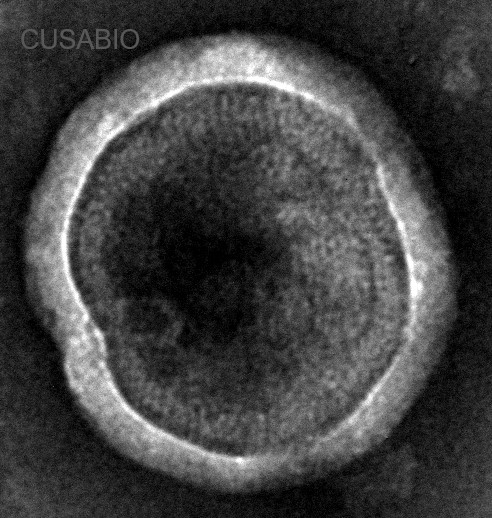
The VLP-like structures of CCR8 has been confirmed by TEM.
参考文献:
[1] Karin, Nathan. "Chemokines and cancer: new immune checkpoints for cancer therapy. "Current opinion in immunology 51 (2018): 140-145.
[2] Das, Suvendu, et al. "Tumor cell entry into the lymph node is controlled by CCL1 chemokine expressed by lymph node lymphatic sinuses." journal of Experimental Medicine 210.8 (2013): 1509-1528.
[3] Whiteside, Sarah K., et al. "CCR8 marks highly suppressive Treg cells within tumours but is dispensable for their accumulation and suppressive function ." Immunology (2021).
[4] Roose, Heleen, et al. "Investigation of the best therapeutic approach to target CCR8 expressed on tumor regulatory T cells to boost anti-tumor immune responses." (2021): 1732-1732.
[5] Korbecki, Jan, et al. "CC chemokines in a tumor: a review of pro-cancer and anti-cancer properties of receptors CCR5, CCR6, CCR7, CCR8, CCR9, and CCR10 ligands." international journal of molecular sciences 21.20 (2020): 7619.











