单抗、多抗、重组抗体应如何选择
日期:2023-07-26 09:26:17
随着生命科学的快速发展,针对蛋白质的研究日益增多,突显了抗体在实验中的重要作用。面对多样且复杂的抗体试剂市场,选择适合实验的抗体尤为重要。在准备购买抗体时,需要考虑许多因素。例如,实验的目的是什么,这种抗体能否在预期的实验应用中使用?这种抗体是否适用于实验中的细胞或组织?
如果您研究的是针对同一目标的单克隆、多克隆或重组抗体,应该如何选择?它们之间有什么区别?是否有一种比其他种类更好,或者它们都是为不同的目的而设计的?这些问题很复杂,但绝对值得探讨。
在本文中,我们将重点介绍这三种抗体及其之间的差异。
1. 多克隆抗体
多克隆抗体(pAbs)是由体内不同B细胞谱系产生的异质混合物,可以识别同一抗原中的多个不同表位。多克隆抗体的生产通常包括收集免疫动物的血液,分离免疫球蛋白,并进行亲和纯化以去除非特异性抗体 [1]。多克隆抗体的生产最常在兔子中进行,但也可以在有蹄类动物(绵羊、山羊、马、猪等)、啮齿类动物和鸡等动物中进行 [2]。与其他物种相比,兔子更容易且成本较低,能对包括小分子和带有或不带有翻译后修饰的多肽在内的各种抗原产生强烈的免疫应答。从兔子获取血液也相对容易。
多克隆抗体具有较弱的特异性、较强的亲和力和较高的敏感性,但容易发生非特异性染色。因此,多克隆抗体特别适用于检测或捕获低丰度抗原。如果表达量不清楚,并且存在经济和时间限制,也可以选择多克隆抗体。多克隆抗体通常用作免疫分析中的二抗,包括ELISA、Western blot和免疫组织化学。在ELISA中,一抗(单克隆抗体)与目标抗原结合,而HRP偶联的二抗(多克隆抗体)用于结合一抗,放大信号从而提高检测效果 [3]。由于相对于单克隆抗体而言,多克隆抗体具有更高的敏感性,因此它们特别适用于癌症或免疫性疾病标记物的早期检测 [4]。由于多克隆抗体通常包含针对某一特定抗原的不同表位,包括对变性抗原具有抗体结合能力的表位,因此它们在深层固定的样本中也能很好地工作。多克隆抗体最常用于石蜡包埋组织切片的染色。此外,在农业生产中,多克隆抗体还用于现场监测农药残留。
2. 单克隆抗体
单克隆抗体是来源于单个B细胞克隆的同种抗体,能够检测抗原中的单个表位。所有单克隆抗体最初都是多克隆抗体混合物,但通过选择或克隆过程进行分离,以鉴定和扩大所需的单价克隆。单克隆抗体通常是从啮齿类动物、兔子和骆驼等宿主中产生,并根据所需抗体类型采用各种方法进行生产。
传统上,单克隆抗体的生产包括用目标蛋白免疫宿主动物,提取能识别和响应抗原的B细胞,然后将B细胞与骨髓瘤细胞融合,形成稳定的杂交瘤细胞,可持续产生目标抗体,最后在细胞培养上清液或小鼠腹水中培养杂交瘤细胞系。由Köhler和Milstein首次提出的杂交瘤技术 [5] 需要进行免疫以产生抗体,并受到个体健康状况、免疫状态等因素的影响,导致所产生的抗体一致性和重复性较差。此外,动物衍生的抗体常常会引起患者的免疫反应,限制了它们作为临床治疗的应用。
单克隆抗体具有较强的特异性,但亲和力和敏感性较低。它们适用于检测相对高表达水平的抗原。由于单克隆抗体能够结合细胞特异性抗原并靶向这些细胞以消除或中和其对机体可能产生的任何有害效应,它们已成为癌症 [6] [7]、各种自身免疫性疾病和其他疾病的有效治疗方法。单克隆抗体广泛用于生物医学研究和医学领域,用于治疗、诊断和研究疾病,以及开发和测试新药。美国食品和药物管理局(FDA)已批准多种单克隆抗体用于治疗,并有数百种正在进行各个阶段的临床试验。
单克隆抗体可用于分析抗原的精细结构和测试抗原与抗体之间的未知结构关系。针对复杂生物混合物中特定分子的抗体可以用于分离、分析和纯化特定的分子抗原。单克隆抗体试剂可用于临床诊断和治疗,包括抗体-药物偶联物 [8] 和针对新兴传染病的疫苗 [9]。
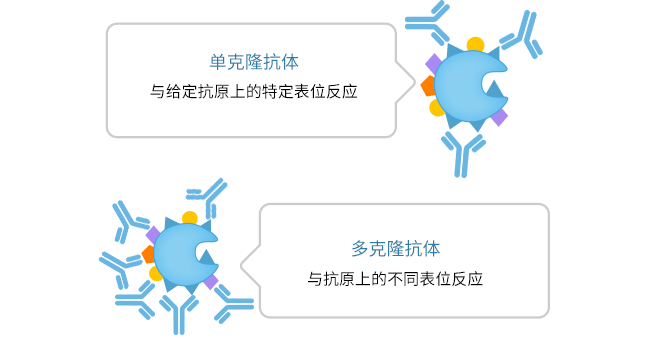
图1. 单克隆抗体和多克隆抗体的主要区别
3. 重组抗体
重组抗体,也称为基因工程抗体,是利用基因重组技术制备的抗体。将抗体基因克隆到表达载体中,然后转染到适合的宿主细胞系中进行抗体表达。重组抗体使得制备人源化抗体和全人源抗体成为可能。哺乳动物细胞系是制备重组抗体最常用的方法,也可以使用细菌、酵母或昆虫来源的细胞系。
与单克隆抗体相比,重组抗体可以在无需免疫的情况下稳定大规模生产。避免了由小鼠来源抗体引起的人体免疫反应。重要的是,重组抗体具有良好的一致性、高重复性和较好的再现性。更多的基因组合可以进行重组,包括抗体片段表达、亚型替代、嵌合抗体、抗体人源化等。重组抗体存在多种形式,从IgG到scFv、Fab或VHH片段,以及双特异性和三特异性变体 [10]。根据治疗需求可以制备新的抗体。由于稳定转染筛选出稳定的细胞系进行体外表达,重组抗体适用于单克隆抗体药物的快速工业化生产。较小的分子量使重组抗体具有更强的穿透能力,因此更容易到达病变的核心部位。重组抗体可以通过原核细胞、真核细胞或植物表达系统大规模生产,大大降低了生产成本。
4. 多克隆抗体、单克隆抗体和重组抗体的优缺点
随着抗体制备技术的快速发展,多克隆抗体、单克隆抗体和重组抗体相继出现。每种抗体都有其独特的优点,也有不可避免的缺点。因此,一些实验将几种抗体串联起来,利用它们各自的优势来获得更好的实验结果。下表列出了三种抗体在不同方面的优缺点。
| 多克隆抗体 | 单克隆抗体 | 重组抗体 | |
|---|---|---|---|
| 重复性 | 较低 | 高;批次间差异小 | 更高;高纯度,批次间差异小 |
| 特异性 | 弱 | 强 | 更强 |
| 生产周期 | 2到3个月的开发和生产周期 | 4到6个月的开发周期;4到6周的生产周期 | 4个月的开发周期;1到6周的生产周期 |
| 动物免疫 | 是 | 是 | 否 |
| 亚型切换 | 困难 | 困难 | 方便 |
| 表达系统 | 常见的哺乳动物细胞(兔子、绵羊、山羊等) | 小鼠腹水法、细胞培养上清法和重组抗体表达系统 | 常见的哺乳动物细胞系,也可以在特殊工程改造的细胞系(酵母、细菌、昆虫和转基因植物)中表达 |
| 成本 | 相对较低 | 生产昂贵;需要更多专业人员操作 | 需要技术专长和大量的时间和金钱投入来生产 |
| 人类免疫反应 | 不可避免 | 不可避免 | 可避免 |
当你准备购买抗体时,除了考虑抗体类型、宿主来源、纯度、免疫原、反应物种、标记物、实验验证应用和支持数据外,还有一些必要的参考因素。合适的抗体可以帮助你获得理想的实验结果。
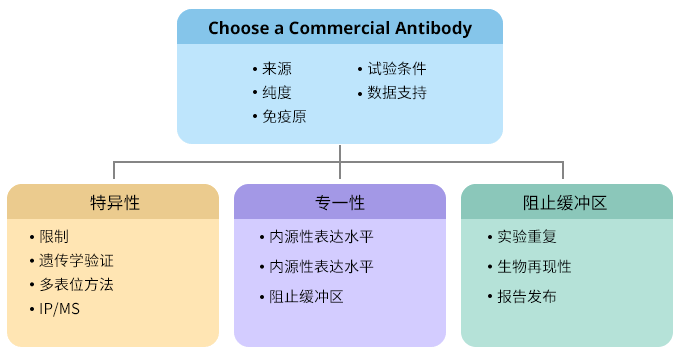
图2. How to choose a commercial antibody
参考文献:
[1] Carey Hanly W, Artwohl JE, Taylor Bennett B. Review of polyclonal antibody production procedures in mammals and poultry [J]. ILAR J. 37(3), 93–118 (1995).
[2] Chiou VY. The development of IgY(DeltaFc) antibody based neuro toxin antivenoms and the study on their neutralization efficacies [J]. Clin. Toxicol. 46(6), 539–544 (2008).
[3] Cox KL, Devanarayan V, et al. Assay Guidance Manual [Internet]. In: Immunoassay Methods. Sittampalam GS, Coussens NP, Brimacombe K et al. (Eds). Eli Lilly & Company and the National Center for Advancing Translational Sciences, MD, USA, 223–266 (2012).
[4] Kulagin AD, L.I, Miloserdov IA, et al. Polyclonal rabbit antithymocyte globulin (thymoglobulin): immunomodulatory effects and new aspects of its clinical application [J]. Ter Arkh, 2010. 82(7).
[5] Köhler G,Milstein C. Continuous cultures of fused cells secreting antibody of predefined specificity [J]. Nature (1975) 256:495–7.
[6] Gharwan H, Groninger H. Kinase inhibitors and monoclonal antibodies in oncology: clinical implications [J]. Nat. Rev. Clin. Oncol. 13(4), 209–227 (2015).
[7] Carvalho S, Levi-Schaffer F, et al. Immunotherapy of cancer: from monoclonal to oligoclonal cocktails of anti-cancer antibodies: IUPHAR Review 18 [J]. Br. J. Pharmacology 173(9), 1407–1424 (2016).
[8] Shepard HM, Phillips GL, et al. Developments in therapy with monoclonal antibodies and related proteins [J]. Clin. Med. (Lond.) 17(3), 220–232 (2017).
[9] Wang Q, Yan J, Fu Gao G. Monoclonal antibodies against Zika virus: therapeutics and their implications for vaccine design [J]. J. Virol. 9, e01049–17 (2017).
[10] Carl A Ascoli & Birte Aggeler. Overlooked benefits of using polyclonal antibodies [J]. BIOTECHNIQUESVOL. 65, NO. 3, 2018.
[11] Lipman NS, Jackson LR, et al. Monoclonal versus polyclonal antibodies: distinguishing characteristics, applications, and information resources [J]. ILAR J. 46(3), 258–268 (2005).











