靶向GPC3在肝癌中初显成效,未来联合治疗潜力更大
日期:2021-05-28 09:57:20
近日,2021年美国临床肿瘤学会ASCO公布了首个靶向 GPC3的4代CART疗法后线治疗肝癌的摘要,其疾病控制率为50%。这项研究首次报道了4G-CAR-GPC3 T细胞单独或与TKIs联合治疗具有可管理的安全性,同时对接受过多种治疗的晚期HCC患者显示了潜在的抗肿瘤活性。早在2020年,华人团队在全球率先开展了以GPC3为靶点的CAR-T细胞治疗晚期HCC的临床试验。数据表明,晚期HCC患者接受CAR-GPC3 T细胞治疗耐受性良好、基本安全可控,罕见严重毒副反应,显示出较好临床获益 [1]。近年来,GPC3的生物学意义已经有较多报道,均证实与肝癌的预后有密切关系,GPC3成为了目前肝癌治疗上最有前景的靶点之一。那么,GPC3是什么?GPC3在肿瘤靶向治疗中的潜力如何?一起来了解一下。
1、GPC3的结构及其功能是什么?
磷脂酰肌醇蛋白聚糖 3(Glypican-3, GPC3),也称MXR7, OCI-5, GTR2-2,是硫酸乙酰肝素糖蛋白(heparan sulfate proteoglycan, HSPG)家族中的一员 [2]。人GPC3基因定位于染色体Xq26.10,是一种由糖基磷脂酰肌醇(GPI)锚定在细胞膜上的HSPG糖蛋白。如 图1所示,GPC3编码580个氨基酸,核心蛋白相对分子质量约为70 kDa [3, 4]。中间为 Furin蛋白酶切位点。有研究提示,GPC3核心蛋白发挥作用,首先要通过Furin蛋白酶裂解Arg 358和Cys 359形成大约40 kDa的N-端蛋白和30 kDa左右含有两条硫酸乙酰肝素(HS)链的C-端蛋白,从而参与调节相关信号通路的传递 [5-7]。
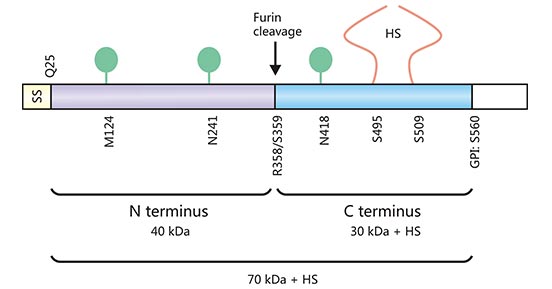
图1. GPC3结构
*图片来源于 European journal of cancer出版物 [4]
GPC3在正常胚胎组织中(包括肝脏和胎盘)高表达,而在成年人正常组织中表达非常低或不表达 [8]。GPC3与肝素结合型蛋白,如细胞外基质成分、细胞粘附分子、生长因子、酶和酶抑制物等相互作用,参与调节细胞分化、增殖、粘附和迁移等生理过程 [9]。大量研究发现,GPC3在肝癌组织中特异性高表达,与肝癌的预后有密切关系。此外,GPC3在黑色素瘤、卵巢透明细胞癌等其他肿瘤也有少量表达 [10, 11]。研究提示,GPC3可能参与多种信号通路,在肿瘤细胞生长中发挥重要生物学功能。
2、GPC3与哪些信号转导通路相关?
目前,大量的研究集中在GPC3在HCC细胞中的特异性表达,但其对癌细胞生长的作用机制尚未明确。如 图2所示,主要存在以下3种理论:1)Hedgehog(Hh)信号通路,GPC3可与Hh结合,导致Hh失去与其受体Ptc的结合能力。Ptc会抑制Smo蛋白活性,从而抑制下游通路;2) Wnt信号通路,GPC3过表可上调c-Myc的表达,c-Myc是经典的Wnt信号通路的蛋白,而c-Myc也可以在转录水平增加GPC3的表达。有研究表明,突变的GPC3可以阻断Wnt信号通路并且抑制Wnt信号通路依赖的肿瘤生长;3)FGF2信号通路,通过免疫共沉淀的方法,有研究发现,GPC3可与FGF2结合,并认为GPC3可抑制 FGF2和 BMP-7的活性,从而抑制肝癌的生长 [12, 13]。
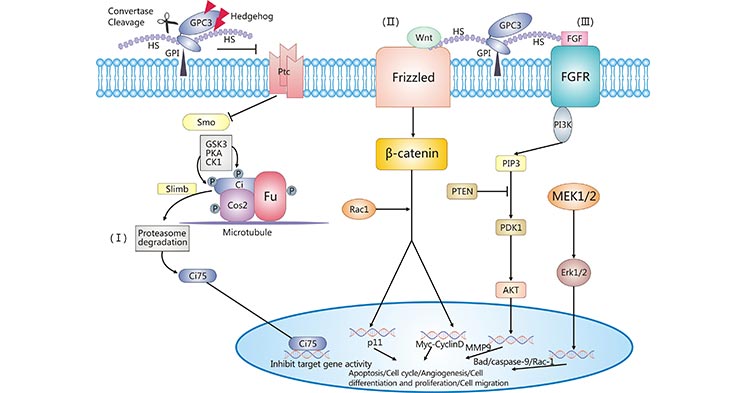
图2. GPC3相关的信号转导通路
*图片来源于 Medicinal research reviews [12]
此外,前面提到,GPC3的C-端含两条HS链,虽然GPC3的HS链没有在GPC3与Wnt和Hh相互作用时发挥其作用,但有研究提示HS可与生长因子FGF2互相作用从而调控细胞生长 [14]。另外有研究认为,GPC3蛋白可与胰岛素样生长因子2(IGF2)和胰岛素样生长因子I型受体(IGFIR)结合,通过IGF2信号途径来诱导肝癌细胞生长 [15]。目前,GPC3在HCC诊断中有很好的检测效果,其作为肝癌诊断生物标志物的价值不容小觑。
3、GPC3在肿瘤中的作用
GPC3作为HCC新的肿瘤标记物,其在肝癌组织中的特异性高表达已被广泛报道。更多的研究发现GPC3还与多种癌症相关,且在肿瘤组织中的表达具有差异性。在非小细胞肺癌、黑色素瘤、卵巢卵黄囊瘤、卵巢透明细胞癌和结肠癌中为高表达。在胃癌、卵巢癌和胆管癌中为低表达 [16, 17],但另有报道GPC3在胃癌中呈高表达 [18]。目前,除HCC以外,GPC3在其他人类肿瘤中的诊断意义有待进一步探究。
在肝癌中,大量数据表明GPC3阳性患者的5年生存率较GPC3阴性患者低 [19-20]。此外,GPC3还是HCC患者根治性切除后,用于预测肿瘤复发和总生存期的一种潜在的、可靠的生物标志物。GPC3低表达的患者一般预后良好,而GPC3高表达被作为癌症复发的危险信号。GPC3作为检测肝癌的标记物,已从诊断标记物的研究扩展到肝细胞癌体内外生长功能及机制的研究。尽管靶向GPC3已成为肝癌治疗的热点,但GPC3在其它肿瘤的作用尚未明确。通过对GPC3与肿瘤关系的深入研究,有望为肿瘤免疫治疗提供新途径。
4、GPC3研发药物及临床前景
目前全球范围内尚无GPC3的靶向药物上市。针对GPC3蛋白的靶向治疗主要包括抗体、抗体-药物偶联物(ADC)、免疫毒素、肿瘤疫苗、靶向肽、嵌合抗原受体、基因治疗等。近年来,研究者们以GPC3为靶点进行了大量药物的研发和细胞治疗研究,其中有一些已经进入了临床试验,如GPC3人源化单克隆抗体GC33、GPC3多肽疫苗、以GPC3为靶点的嵌合抗原受体修饰T细胞(CAR-T)等(参见下表)。
| 药物名称 | 全球最高研发状态 | 原研公司 | 治疗领域/适应症 | 最后更新日期 |
|---|---|---|---|---|
| ECT-204 | 临床二期 | / | 肝癌;
肝细胞癌; |
2021-05-06 |
| Anti-GPC3 chimeric antigen receptor T cell therapy (Shanghai Genechem) | 临床二期 | 上海吉凯基因医学科技股份有限公司; | 肝癌;
肝细胞癌; |
2020-12-18 |
| Anti-CD3/MUC1-armed cytokine induced killer cells | 临床二期 | 本康生物制药(深圳)有限公司; | 肺癌;
肝癌; 结直肠癌; 乳腺癌; 肾细胞癌; 胃癌; 胰腺癌; |
2020-12-18 |
| Codrituzumab/GC33 | 临床二期 | 中外制药株式会社;
罗氏; |
肝细胞癌; | 2020-08-28 |
| GPC-3298306 | 临床二期 | National Cancer Center Of Japan; | 肝细胞癌;
卵巢癌; |
2020-08-28 |
| ERY-974 | 临床一期 | 中外制药株式会社; | 实体瘤; | 2020-08-28 |
| GPC3-CAR-T cell therapy (Beijing Tsinghua Chang Gung Hospital) | 临床一期 | 北京清华长庚医院; | 肝细胞癌; | 2020-12-18 |
| MDX-1414 | 临床一期 | 百时美施贵宝; | 肿瘤; | 2020-08-28 |
| Anti-GPC3 chimeric antigen receptor T cell therapy (Hunan Yongren Medical Innovation/Guangdong Zhaotai InVivo Biomedicine) | 临床一期 | 湖南昭泰医疗集团有限公司; | 肺癌;
肝癌; |
2020-12-18 |
| GPC3-CAR-T cell therapy(靶向磷脂酰肌醇蛋白多糖-3嵌合抗原受体修饰的自体T细胞) | 临床一期 | 科济生物医药(上海)有限公司; | 实体瘤;
肝细胞癌; 鳞状细胞癌; |
2020-08-28 |
| Anti-GPC3 CAR T-cell therapy (Nanjing University) | 临床一期 | 南京大学; | 肝细胞癌; | 2020-12-18 |
| GLYCAR T cell therapy (Baylor College of Medicine) | 临床一期 | 贝勒医学院; | 肝细胞癌; | 2020-08-28 |
| GPC3-T2 CAR-T cell therapy (The Second Affiliated Hospital of Guangzhou Medical University) | 临床一期 | 广州医科大学附属第二医院; | 肝细胞癌;
鳞状细胞癌; |
2020-12-18 |
| B010-A | 临床阶段不明 | 上海医药集团股份有限公司; | 肝细胞癌; | 2021-03-15 |
| GPC3 CAR-T(HuaDao CAR-Tcell) | 临床前 | 华道(上海)生物医药有限公司; | 肝细胞癌; | 2020-08-28 |
| GPC3-CART(Shanghai Unicar-Therapy Bio-Medicine Technology) | 临床前 | 上海优卡迪生物医药科技有限公司; | 肝癌; | 2020-12-18 |
| HLX-63 | 临床前 | 上海复宏汉霖生物医药有限公司; | 实体瘤; | 2021-01-04 |
| LQ-102 | 临床前 | / | 肝细胞癌; | 2021-02-04 |
数据来源于:药渡
GC33(Codrituzumab)是首个靶向GPC3的抗体,但临床试验的数据显示,GC33并不能完全消除HCC细胞。此外,基于GPC3治疗HCC的肿瘤疫苗GPC-3298306,已经进入II临床期的试验阶段,目前无法查询到上述临床试验的结果。在靶向GPC3的CAR-T细胞免疫治疗中,已有临床结果表明,靶向GPC3的CAR-T细胞可以抑制HCC生长,被认为是一种很有前景的细胞治疗方法。
越来越多的证据显示GPC3是肿瘤药物开发一个有吸引力的靶点选择,是改善肿瘤患者预后有潜能的分子靶标。尽管GPC3在HCC细胞生长方面的分子信号通路并没有完全被阐明,但作为生物标志物,GPC3在HCC的早期诊断、预后判断和免疫治疗中的价值已经逐步显现。在GPC3靶点上进行深度挖掘,结合抗体、疫苗和CAR-T等免疫治疗手段,有望为癌症的有效治疗提供新方向。
5、GPC3科研产品服务
Recombinant Human GPC3 (G537R), partial (Active) (CSB-MP009705HU(M))
GPC3 Antibody (ELISA, WB, IF)(CSB-RA009705A0HU)
Human GPC3 ELISA Kit (CSB-E11333h)
GPC3蛋白
Recombinant Human Glypican-3(GPC3)(G537R),partial (Active) (CSB-MP009705HU(M))
-SDS.jpg)
(Tris-Glycine gel) Discontinuous SDS-PAGE (reduced) with 5% enrichment gel and 15% separation gel.
-AC1.jpg)
Immobilized human GPC3 (G537R) at 5 μg/ml can bind Anti-GPC3 recombinant antibody, the EC 50is 4.739-7.092 ng/ml.
参考文献:
[1] Shi, Donghua, et al. "Chimeric antigen receptor-glypican-3 T-cell therapy for advanced hepatocellular carcinoma: Results of phase I Trials." Clinical Cancer Research 26.15 (2020): 3979-3989.
[2] Feng, Mingqian, et al. "Recombinant soluble glypican 3 protein inhibits the growth of hepatocellular carcinoma in vitro." International journal of cancer. journal international du cancer 128.9 (2011): 2246.
[3] Zong, Jingjing, Zhe Fan, and Yewei Zhang. "Serum Tumor Markers for Early Diagnosis of Primary Hepatocellular Carcinoma. "Journal of Hepatocellular Carcinoma 7 (2020): 413.
[4] Ho, Mitchell, and Heungnam Kim. "Glypican-3: a new target for cancer immunotherapy. "European journal of cancer 47.3 (2011): 333- 338.
[5] Nishida, Takahiro, and Hiroaki Kataoka. "Glypican 3-targeted therapy in hepatocellular carcinoma. "Cancers 11.9 (2019): 1339.
[6] Montalbano, Mauro, et al. "Role of Glypican-3 in the growth, migration and invasion of primary hepatocytes isolated from patients with hepatocellular carcinoma." Cellular Oncology 41.2 (2018): 169-184.
[7] Filmus, Jorge, and Mariana Capurro. "Glypican-3: a marker and a therapeutic target in hepatocellular carcinoma. "The FEBS journal 280.10 (2013): 2471-2476.
[8] Ou-Yang, Robin J., et al. "Expression of glypican 3 in placental site trophoblastic tumor." Diagnostic pathology 5.1 (2010): 1-6.
[9] Pan, Zhijian, et al. "Overexpression of GPC3 inhibits hepatocellular carcinoma cell proliferation and invasion through induction Molecular medicine reports 7.3 (2013): 969-974.
[10] Maeda, Daichi, et al. "Glypican-3 expression in clear cell adenocarcinoma of the ovary." modern pathology 22.6 (2009): 824-832.
[11] Nakatsura, Tetsuya, et al. "Identification of glypican-3 as a novel tumor marker for melanoma." clinical cancer research 10.19 ( 2004): 6612-6621.
[12] Zhou, Fubo, et al. "Glypican-3: A promising biomarker for hepatocellular carcinoma diagnosis and treatment." medicinal research reviews 38.2 (2018): 741-767.
[13] Midorikawa, Yutaka, et al. "Glypican-3, overexpressed in hepatocellular carcinoma, modulates FGF2 and BMP-7 signaling. " International journal of cancer 103.4 (2003): 455-465.
[14] Nakano, Kiyotaka, et al. "Anti-glypican 3 antibodies cause ADCC against human hepatocellular carcinoma cells. "Biochemical and biophysical research communications 378.2 (2009): 279-284.
[15] Sung, Young Kwan, et al. "Glypican-3 is overexpressed in human hepatocellular carcinoma." cancer science 94.3 (2003): 259-262.
[16] Murthy, Siva S., et al. "Expression of GPC3, an X-linked recessive overgrowth gene, is silenced in malignant mesothelioma." Oncogene 19.3 (2000): 410-416.
[17] Peters, M. G., et al. "Inhibition of invasion and metastasis by glypican-3 in a syngeneic breast cancer model." Breast cancer research and treatment 80.2 (2003): 221-232.
[18] Lin, Qiang, et al. "Expression of GPC3 protein and its significance in lung squamous cell carcinoma." medical oncology 29.2 (2012) : 663-669.
[19] Li, B., et al. "Diagnostic value of glypican-3 in alpha fetoprotein negative hepatocellular carcinoma patients. "African health sciences 13.3 (2013): 703-709.
[20] Ning, Su, et al. "Glypican-3, a novel prognostic marker of hepatocellular cancer, is related with postoperative metastasis and recurrence in hepatocellular cancer patients." Molecular biology reports 39.1 (2012): 351-357.
上一篇: 技术|制备抗体时抗原的选择











