细胞因子风暴和病毒感染 你必须知道的
日期:2023-12-21 15:15:42
在2020年1月25日,曹彬教授的团队发表了一篇名为《中国武汉地区感染2019年新型冠状病毒患者的临床特点》的研究论文。该论文揭示了严重患有SARS-CoV-2(以前称为:2019-nCoV)的患者免疫系统存在致命的细胞因子风暴。那么什么是细胞因子风暴?为什么病毒会引起细胞因子风暴,以及其机制是什么?是否有细胞因子风暴的治疗方法?在本文中,我们将专注于病毒感染引起的细胞因子风暴。我们将从以下几个方面为您解释:
1. 什么是细胞因子风暴?
细胞因子风暴,也被称为高细胞因子疾病,是一个健康而强大的免疫系统的全身性表达,导致释放超过150种炎症介质,如TNF-α、IL-1、IL-6、IL-12、IFN-α、IFN-β、IFN-γ、MCP-1和IL-8等。血清中既有促炎细胞因子,也有抗炎细胞因子的升高,这些细胞因子之间的激烈而常常致命的相互作用被称为“细胞因子风暴”。
这是由细胞因子与免疫细胞之间的正反馈循环引起的严重过度免疫反应。症状包括高热、红肿、严重疲劳和恶心,有时可能导致致命后果。细胞因子风暴是急性呼吸窘迫综合症和多器官功能衰竭的重要原因(图1)。
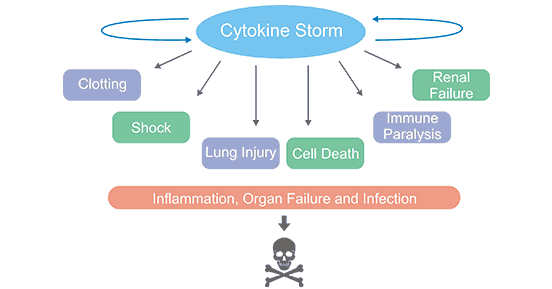
图1. 细胞因子风暴导致直接器官损伤
2. 为什么病毒侵袭会引发细胞因子风暴?
病毒通过受体介导的内吞作用进入宿主目标细胞,大量增殖繁衍,然后通过出芽或诱导编程性细胞死亡释放更多病毒。这些释放的病毒被宿主免疫细胞上的模式识别受体所识别。随后,免疫细胞通过一系列信号传导释放大量细胞因子,激活更多免疫细胞,参与病毒的清除。
然而,正如你所知,免疫是一把双刃剑。当机体的免疫激活试图清除异质性致病微生物时,也会导致机体自身的损伤。如果病毒数量庞大,免疫力强大,会导致更严重的局部抗争,引发局部炎症和细胞损伤,即细胞因子风暴。此时,病情可能会恶化。
以埃博拉病毒为例,它通过潜伏在宿主未成熟的树突状细胞、巨噬细胞等中,逃避免疫系统的识别。经过大量复制和迅速传播,导致多器官细胞坏死和分解。当埃博拉病毒随着分解的细胞一起释放出来时,免疫系统会迅速识别。由于病毒数量庞大,免疫系统被充分激活,释放大量促炎细胞因子、组织因子和血管活性肽。这些释放的因子导致穿透血管壁,释放大量一氧化氮,造成血管壁的继发性损伤,破坏凝血系统。这些反应将引起体内发热、内出血,最终导致多器官功能衰竭(图2)。
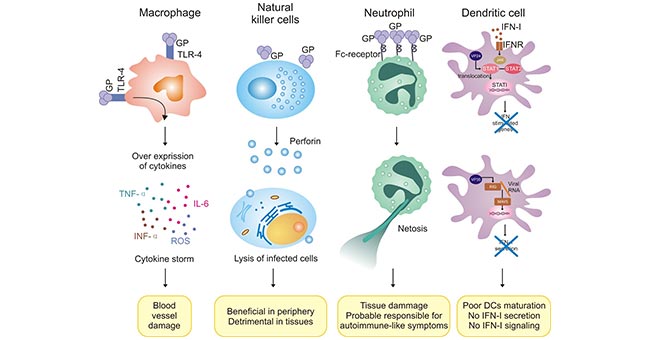
图2. 先天免疫细胞在埃博拉病毒感染中的异常调控
3. 病毒与细胞因子风暴
细胞因子风暴在病毒感染、某些药物以及造血系统疾病中较为常见。细胞因子风暴是急性呼吸窘迫综合症(ARDS)和多器官功能衰竭的重要原因之一。在许多疾病中,它也是死亡的重要原因之一,并且近年来引起越来越多的关注。在本文中,我们主要关注由病毒感染引发的细胞因子风暴。除埃博拉病毒外,登革热病毒、高致病性禽流感病毒(H5N1、H1H1等)、巨细胞病毒、天花病毒、SARS病毒和MERS病毒均可引发细胞因子风暴。
3.1 SARS病毒与细胞因子风暴
严重急性呼吸综合症(SARS)是由SARS冠状病毒感染引起的高热、干咳和胸闷等主要症状。这起事件始于2002年12月。关于SARS引发的细胞因子风暴,香港大学的裴宇翔博士在尸检中发现,严重SARS患者的肺组织受损严重,肺泡中存在多核巨细胞,肺泡巨噬细胞核内的两性染色质结合蛋白染色阳性增多。这些细胞可以分泌TNF、IL-1、TGF等细胞因子,然后诱导成纤维细胞激活、细胞外基质沉积和肺泡上皮损伤修复。肺组织中红细胞的吞噬现象表明,细胞因子调节失控。据推测,SARS感染引发了许多炎症介质的释放。
刘志英检测到治愈和死亡SARS患者体内存在大量炎症和抗炎因子。高水平的IL-6、IL-8和IL-10表明这三种细胞因子在疾病进展中发挥重要作用。在SARS患者的治疗中,常常使用类固醇激素来抑制细胞因子的释放,减少免疫反应并降低死亡率。
正如在《2019新型冠状病毒》一文中所提到的,SARS-CoV-2与2002年的SARS-CoV序列相似度约为70%,与MERS-CoV相似度约为40%。SARS-CoV-2是一种新的冠状病毒毒株,之前在人类中从未发现过。感染冠状病毒的人通常表现出呼吸症状、发热、咳嗽、呼吸急促和呼吸困难。在更严重的情况下,感染会引发肺炎、严重急性呼吸综合症、肾功能衰竭,甚至导致死亡。2019-nCoV感染引发了严重的肺炎疫情。感染者大多是健康人和年轻成年人,症状类似于SARS。部分患者会在病情从轻微转为严重时出现突然变化,细胞因子风暴成为不可忽视的问题。
3.2 流感病毒与细胞因子风暴
流感病毒引发小鼠胶质细胞细胞因子风暴。周建祥等分离培养了新生小鼠脑皮层的胶质细胞,分别在6小时和24小时内体外感染星形胶质细胞和小胶质细胞的甲型H1N1和H3N2流感病毒。收集上清液并通过超滤分子保留去除流感病毒。分别用不同培养时间的条件上清液刺激星形胶质细胞和小胶质细胞。24小时后提取RNA并进行逆转录,用实时荧光定量PCR检测前炎性因子(TNF-α、IL-1β和IL-6)和趋化因子(IP-10、MCP-1和MIP-1)。
该研究表明,不同培养时间的条件上清液可上调正常胶质细胞中的前炎性因子TNF-α、IL-1β、IL-6和趋化因子IP-10、MCP-1、MIP-1,上调程度不同产生细胞因子级联效应。甲型H1N1和H3N2流感病毒感染的星形胶质细胞引发的细胞因子级联效应可能与免疫病理性损害有关。
3.3 EBV与细胞因子风暴
EBV相关的淋巴细胞增殖性疾病与细胞因子风暴有关。EBV相关淋巴细胞增殖性疾病(CAEBV)被称为EBV+LPD,于2008年9月8日至9日在美国国立卫生研究院举行的EBV-LPD研讨会上提名。EBV+LPD分为B细胞型(EBV+B-LPD)和T/NK细胞型(EBV+T/NK-LPD)。也称为出血性综合征(HPS)。木村等分析了39例T-CAEBV和NK-CAEBV患者的病毒学差异和细胞因子分泌情况。他们发现IL-1β、IL-10和IFN-γ在血清中高度表达,但NK细胞型感染患者的IL-13水平高于T细胞型,部分进展为HPS的患者血清表达IL-1β和IFN-γ。此外,19例CAEBV患者的外周血单个核细胞中的细胞因子转录如IL-1α、IL-1β、IL-10、IL-12p35、IL-13、IL-15、TNF-α和IFN-γ增加。
此外,石井等发现单核细胞可以通过细胞膜上的IL-15促进EBV相关NK/T细胞增殖并分泌LMP1,展示了IL-15在EBV-LPD疾病进展中的重要作用。SNK6细胞系高度表达IFN-γ、IL-9和IL-10。IL-10通过促进LMP1和CD25的分泌间接促进细胞增殖。不同类型的EBV-LPD表达不同的细胞因子。
4. 是否有细胞因子风暴的治疗方法?
目前,细胞因子风暴的治疗主要包括以下四项措施:
- 抗休克疗法(症状治疗,救命第一):输液以确保血容量,应用血管活性药物,必要时进行机械通气,保护重要器官功能;
- 支持和症状治疗(恢复体力):常规输液,维持水、电解质和酸碱平衡,营养支持等;
- 抑制过度的免疫细胞活化和细胞因子产生(痊愈,寻求康复):在临床上,常常使用激素治疗(肾上腺皮质激素等)以适当的剂量和方法,以及非甾体抗炎药和自由基清除剂(大量维生素C、维生素E等)。
- 抗体中和细胞因子风暴(精准治疗):使用中和升高的细胞因子的单克隆抗体,以防止严重疾病和死亡。
5. 是否有细胞因子风暴的药物?
根据细胞因子风暴的机制,药物开发的思路源于以下原则:
- 减少活化的细胞因子,如IL-12、IFN-γ、TNF-α等;
- 增加抑制性细胞因子,如IL-10、TGF-β等;
- 减少白细胞进入炎症组织,如1-磷酸鞘脂(S1P)。
研究人员从以上三个思路进行了大量研究工作,研究了各种皮质类固醇、PPAR激动剂、S1P1受体激动剂、COX抑制剂、抗TNF抗体、ACEI / ARB抑制剂和OX40抑制剂等对抗细胞因子风暴的药物。在上述治疗方法中,目前在动物实验中效果最好的与肺炎相关的细胞因子风暴治疗是1-磷酸鞘脂受体1激动剂(S1PR1)。
磷酸鞘脂-1-磷酸(S1p)是一种信号性的鞘脂,具有五个亚型的受体,在肺组织中主要在血管内皮细胞和淋巴细胞中表达。S1P1激动剂(CYM-5442和RP-002)已被报道通过减轻细胞因子和抑制先天免疫细胞的浸润,保护小鼠免于严重流感感染引起的死亡。
在2009年H1N1大流行性流感的小鼠模型中,单独的S1P1受体激动剂可将致命感染引起的死亡率降低80%以上。此外,与奥司他韦的联合使用可以将小鼠的死亡率降低96%。这是迄今为止在治疗病毒引发的细胞因子风暴时使用免疫调节策略取得的最好效果。
目前,诺维诺的Siponimod,一种鞘脂-1-受体调节剂药物,已获得多发性硬化症的治疗批准。因此,Siponimmod能否用于SARS-CoV-2病毒感染引起的严重肺炎?与瑞德西韦相比,获批的西泮酮具有更好的安全性,并且与在危重病人中大量使用激素相比,靶向性的西泮酮副作用更小,它是否与洛匹那韦/利托那韦等抗病毒药物一起使用会效果更好?让我们期待未来的科研。
参考文献:
[1] Huang C, Wang Y, et al. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China [J]. Lancet, 2020 Jan 24.
[2] Parsi M, Dargan K. Hemophagocytic Lymphohistiocytosis Induced Cytokine Storm Secondary to Human Immunodeficiency Virus Associated Miliary Tuberculosis[J]. Cureus 2020 Jan 07;12(1).
[3] Benjamin G. Chousterman, et al. Cytokine storm and sepsis disease pathogenesis[J]. Seminars in Immunopathology. July 2017, Volume 39, Issue 5, pp 517–528.
[4] Huang KJ, Su IJ, et al. An interferon-gamma-related cytokine storm in SARS patients [J]. J. Med. Virol. 2005 Feb;75(2).
[5] Sun Y, Jin C, et al. Host cytokine storm is associated with disease severity of severe fever withthrombocytopenia syndrome[J]. INFECT DIS. 2012, 7 (206).
[6] IshiiH, Takahara M, et al. Monocytes enhance cell pro-liferation and LMP1 expression of nasalnatural killer/T-cell lympho-ma cells by cell contact-dependent interactionthrough membrane-bound IL-15 [J]. Int J Cancer. 2011, 130 (1): 48-58.











