IF= 64.5 | Cell 朱书等人发现Gasdermin D可以通过调节MHCII水平诱导小肠维持对食物的耐受性
浏览次数:22 日期:2023-07-28 14:11:47
肠上皮细胞(IEC)构成宿主细胞和众多外来抗原之间的主要屏障;目前尚不清楚IEC是如何诱导针对病原体的保护性免疫,并同时维持对食物的免疫耐受。近日,中国科技大学朱书教授团队在肠道免疫研究中取得新进展,于2023年6月在CELL杂志发表了一文Gasdermin D licenses MHCII induction to maintain food tolerance in small intestine,在对GSDMD在食物耐受中的功能进行详细分析后,作者有了新的发现,ICE积累了一个未被熟知的 GSDMD 13-kD N 端片段,该片段由于 caspase-3/7 响应饮食抗原而裂解。作者通过小鼠对比试验,证明GSDMD 的差异裂解可以被认为是控制小肠免疫与耐受的调节枢纽。

近年来,Cleaved Gasdermin D (GSDMD)蛋白作为介导细胞焦亡的关键执行蛋白引起了科学界的广泛关注(细胞焦亡:pyroptosis,是细胞死亡的一种裂解形式,可引发细胞自杀,是针对外来抗原的免疫防御的一个重要方面)。当细胞受到病原相关分子模式(PAMPs)和损伤相关分子模式(DAMPs)的刺激时,细胞内的信号感受器会通过炎症小体(inflammasome)的依赖或非依赖机制激活caspase-1/4/5/8/11,从而切割GSDMD的N端,产生p30片段。这一过程进而导致细胞膜成孔、细胞焦亡和炎性因子的释放。
这些功能主要是在髓系细胞研究中被发现,但在生理状态下,GSDMD在多种组织器官中广泛表达。作为gasdermin家族的成员,GSDMD在肠道尤其是小肠中表达丰富。因此,人们迫切希望了解GSDMD在肠道以及其他组织中的非焦亡功能,以及它在肠道中具体发挥的生理作用。
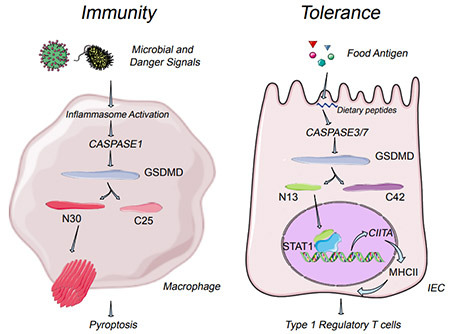
图1. GSDMD分子在不同的细胞中呈现双重免疫特性:对抗病原体,在细胞膜上形成孔穴,参与免疫激活;对食物抗原,进入细胞核,参与转录,从而诱导免疫耐受。
研究人员首先对不同组织细胞中的GSDMD进行了蛋白印迹检测,发现检测的各组织样品中只有在小肠的IEC中能检测到一条大约13kD大小的剪切带。进一步的研究表明,这个剪切带是由食物抗原刺激下的十二指肠IECs中的CASPASE-3/7切割GSDMD的N端的88位天冬氨酸(人源GSDMD是87位)而产生的,并依此构建了GSDMD的小肠剪切突变GsdmdSICR鼠以进行后续研究。
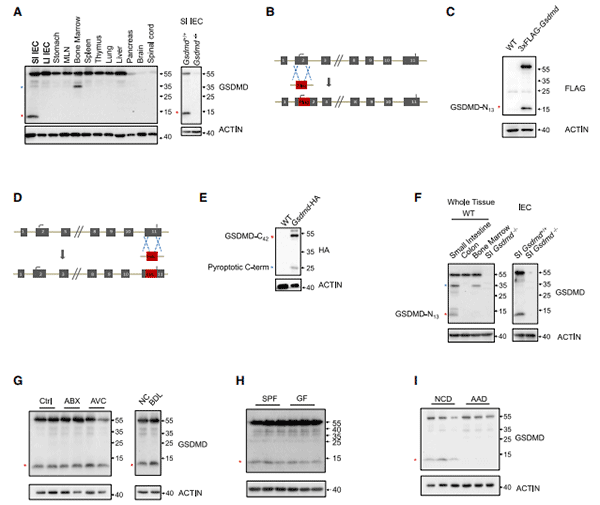
图2. CASP3/7在食物抗原诱导下切割GSDMD 88位天冬氨酸产生N13片段
那么,GSDMD的这一剪切带具体在小肠中发挥着什么作用?研究人员首先构建了GSDMD的N13以及对应的C42片段的荧光质粒,他们发现N13片段会进入细胞核,并且怀疑核孔复合体的蛋白成员可能协助其进入细胞核。通过比对野生鼠和GSDMD 敲除鼠的前端小肠IEC的RNA 测序结果,研究人员发现GSDMD敲除会导致IEC的二类分子与二类分子的转录因子CIITA和MHCII的水平下降。
j9九游会登录入口首页生物(Cusabio)助力论文发表:
针对这一现象,作者使用多种基因编辑以及特殊处理小鼠前端小肠IEC的二类分子进行FACS和qPCR实验进行论证,结果证实:GSDMD的N13片段缺失会导致前端小肠IEC的二类分子表达水平显著降低。后续的单细胞RNA测序结果证实,生理状态下的这一变化只会发生在IEC中,对于其他经典的抗原递呈细胞(包括B细胞和髓系细胞)则没有影响。
此外通过单细胞RNA测序结果,研究人员发现,在N13片段缺失后,前端小肠的Tr1细胞明显减少,qPCR和FACS试验结果进一步佐证了N13片段缺失造成IEC二类分子下降从而导致Tr1细胞减少。由于Tr1细胞是一群免疫抑制型的CD4+ T细胞,并且被认为是诱导食物耐受的关键细胞之一,结合N13片段是由食物诱导产生且前端小肠具有营养物质的消化吸收的生理功能,研究人员猜测N13片段最终参与诱导食物耐受过程。为此,研究人员针对多种基因表达背景小鼠构建了两组食物耐受模型,花生提取物诱导的花生过敏模型以及OVA诱导的迟发型超敏反应模型,结果表明,无法产生N13片段的GsdmdSICR鼠、IEC MHCII在IEC特异敲除以及Tr1缺失的小鼠都对食物表现出强烈的过敏反应。
这项研究为我们理解GSDMD在肠道中的非焦亡功能提供了重要线索,说明GSDMD维持宿主肠道稳态发挥了重要作用,并揭示了其在食物耐受中的潜在作用,为食物过敏的治疗手段提供新思路。
j9九游会登录入口首页生物(Cusabio)助力论文发表:
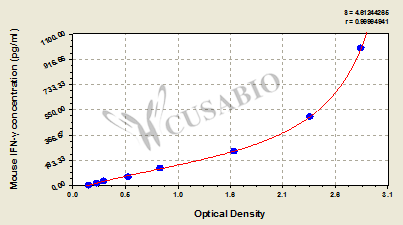
Mouse Interferon g, IFN-g ELISA Kit(CSB-E04578m)
Evaluation of the protective immune response of an attenuated strain of Toxoplasma gondii with long-term passages on the Gecko cell line RR Ronizi,Veterinary parasitology, 2023
A probiotic bi-functional peptidoglycan hydrolase sheds NOD2 ligands to regulate gut homeostasis in female mice J Gao, Nature communications, 2023
Gasdermin D licenses MHCII induction to maintain food tolerance in small intestine K He, Cell, 2023
更多相关文献请点击 >>










