Advanced Science | ATP13A1调控MAVS介导的抗病毒免疫反应的分子机制
浏览次数:30 日期:2023-01-18 11:28:05
天然免疫是机体免疫系统的重要组成部分。当机体受到外源病原体的入侵时,天然免疫中的多种模式识别受体(pattern recognition receptors,PRRs)可以通过感知病原体相关分子模式(pathogen-associated molecular patterns,PAMPs)来引发细胞中信号通路的激活,从而清除病原体以维持细胞的稳态。
j9九游会登录入口首页生物ELISA试剂盒助力老师发文:

RIG-I-MAVS信号通路是天然免疫中一条重要的信号通路。位于胞质中的RIG-I分子主要识别带有5’三磷酸的单链或双链RNA,以及带有5’双磷酸的双链RNA。当RIG-I分子感知到外源RNA时,就会通过构象变化促使其CARD结构域发生多聚化,并进一步促进位于线粒体外膜上的MAVS分子聚集。随后,活化的MAVS分子进一步激活下游的转录因子,促进I型干扰素的产生。RIG-I-MAVS信号通路在细胞中受到严格地调控,以避免激活不足或者过度激活对机体造成的损伤。除了目前已发现的翻译后修饰和调控因子外,是否还存在其他未知分子参与RIG-I-MAVS信号通路的调控。近期发表于国际学术期刊Advanced Science上的一篇研究成果“The Endoplasmic Reticulum ATP13A1 is Essential for MAVS-mediated Antiviral Innate Immunity”给出了答案。

文献来源:https://onlinelibrary.wiley.com/doi/abs/10.1002/advs.202203831
张瑞博士团队通过全基因组CRISPR-Cas9敲除筛选体系,发现位于内质网上的ATP13A1蛋白参与调控RIG-I-MAVS信号通路。结合qPCR、ELISA、Western blot、组分分离和免疫荧光等多种方法,研究人员在多种细胞中探究了ATP13A1发挥作用的具体机制。ATP13A1敲除的细胞与野生型细胞相比,其在病毒感染时所产生的I型干扰素显著降低,抗病毒能力也明显下降。进一步地实验表明ATP13A1缺失的细胞中MAVS会发生蛋白酶介导的降解,同时MAVS激活下游信号分子的能力也明显受到影响。在髓系细胞中特异性敲除Atp13a1的小鼠,其对RNA病毒感染更敏感,抗病毒能力也明显下降。总之,该研究发现内质网蛋白ATP13A1通过影响线粒体蛋白MAVS的稳定性和活性来进行有效的抗病毒免疫反应调控。
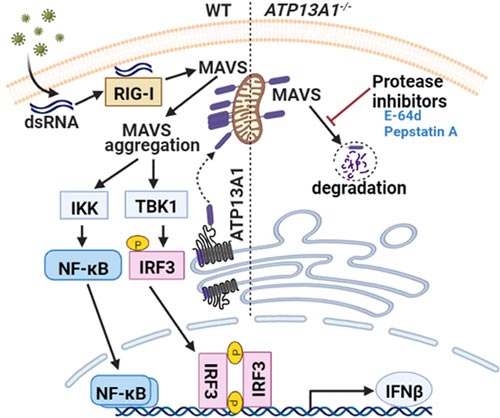
已获得原作者授权
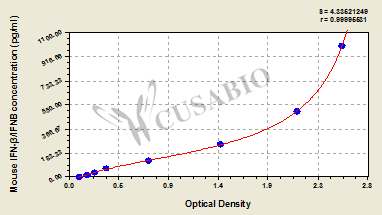
Mouse Interferon β,IFN-β/IFNB ELISA Kit
中文名称:小鼠β干扰素(IFN-β/IFNB)ELISA Kit
货号:CSB-E04945m
规格:96T/48T
标准曲线:
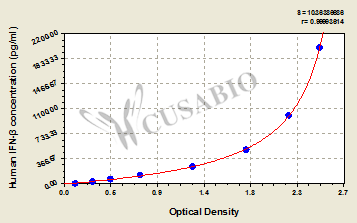
Human Interferon β,IFN-β/IFNB ELISA Kit
中文名称:人β干扰素(IFN-β/IFNB)ELISA Kit
货号:CSB-E09889h
规格:96T/48T
标准曲线: